医疗器械研发:光控向导RNA进行CRISPR靶向
在科学界,基因编辑技术CRISPR自问世以来就开创了属于自己的时代,它在医学科研领域的应用可以说是百花齐放和硕果累累。
可控制的基因编辑具有改变疾病治疗的作用,也是科学家们研究遗传学的好工具。CRISPR-Cas9基因编辑系统已被证明是一项关键性的发展,因为它可以轻松而精确地进行针对性的基因改变。目前,有两个独立的团队证明了CRISPR-Cas9在特定时间内仅在培养的细胞的子集和斑马鱼胚胎中可以被激活,方法是比之前更严格地用光控制系统。与之前的研究不同的是研究小组的方法靶向CRISPR-Cas9系统中被称为引导RNA的一部分。

光作为控制细胞培养或组织中基因编辑的开关具有众多优势:它具有微创,快速工作的作用,并且与生化控件不同,它不需要向细胞中添加其他化学试剂。操纵基因编辑时间和地点的能力可以帮助研究人员仅在靶向器官内细胞的子集或者胚胎发育过程中的特定时间操纵基因。研究人员已经开发出多种光激活的CRISPR-Cas9系统,所有这些系统都涉及到光控制的Cas9蛋白,但是很难进行其他升级来提高基因编辑对光控蛋白的选择性或效率。匹兹堡大学的亚历山大· 戴特斯说最好的办法是在其他地方添加灯光控制,以使研究人员更自由地设计Cas9。因此,研究小组专注系统的一部分,即引导RNA的部分,该RNA与要切割的DNA序列结合,从而形成Cas9酶识别并剪断DNA-RNA复合物。在新的研究中,卡洛林斯卡研究所的Deiters和Molly M. Stevens带领的研究小组对引导RNA分子进行了修饰,使它们携带的光敏分子“笼罩”了RNA以防止DNA配对。当暴露在正确波长的光下时,笼状分子被切割掉,RNA可以与靶DNA结合,从而启动基因编辑过程。
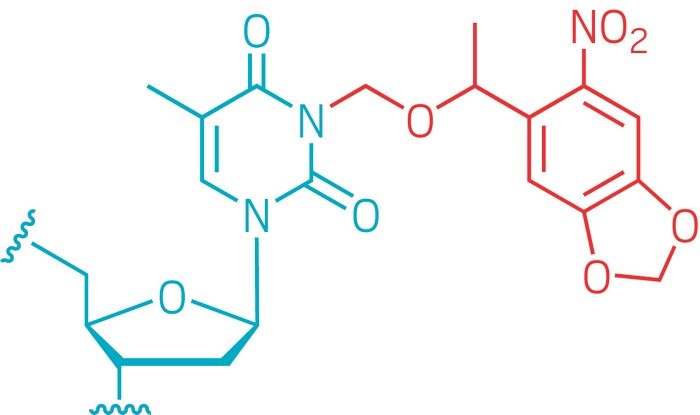
Broad研究所的化学生物学家阿米特·乔杜里在谈到Stevens小组的研究时说:“他们基本上在成功配对的RNA碱基上安装了这种光可切割的旋钮,这是Cas9切割DNA必不可少的。在没有光线的情况下,配对不会发生,而且背景活动非常少。”
研究人员用光老化核糖核酸处理培养的人类细胞,在没有光线的情况下没有发现DNA编辑的迹象。在Stevens小组的实验中,被激活的RNA恢复了70%的基因编辑活性,而对照RNA分子缺少光活性附着物。两个小组在斑马鱼胚胎中测试了他们的系统,发现他们可以通过照亮一只眼睛来引入突变。牛津大学的Lapatrada Taemaitree和tombrown在《透视》杂志上写道,类似的两项独立研究的结果令人满意的,该方法将被证明是可重复的。原则上,可以开发多色靶向系统来允许不同基因同时或在不同时间关闭。

总的来说,CRISPR非常强大,正在为大多数实验室的日常工作带来革命性变化,强大的基因编辑能力迅速让其从基础研究转化到临床试验,从最初的研究工具转变为在疾病治疗中使用的新疗法。目前,科学家们已经使用CRISPR-Cas9编辑人类胚胎中引发疾病的突变。
ITL集团作为新技术创新与优化改进产业化的研发型企业,在医疗领域拥有43年的医疗器械研发经验,经历了很多高端医疗技术的发展和更迭,凭借独特的见解和长期的经验善于整合新技术研发和优化仪器性能。自公司成立以来已经成功研发出400多种医疗产品,如今,ITL也同样希望运用这项技术创造出能够造福人类,改善人类健康,提高人类生活质量的优秀医疗产品。











